Thông tin thuốc tháng 02/2025
1. Tổng quan số lượng báo cáo ADR của Bệnh viện Từ Dũ
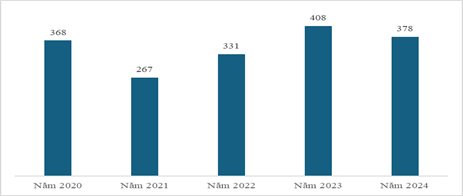
Hình 1. Số lượng báo cáo ADR tại Bệnh viện Từ Dũ giai đoạn năm 2020 - 2024
Trong năm 2024:
- Bệnh viện đã thực hiện 378 báo cáo ADR, giảm 7,9% so với năm 2023 (408 báo cáo), tăng 14,2% so với năm 2022 (331 báo cáo).
- Số lượng báo cáo ADR ngoại trú là 18 báo cáo, giảm 3,6 lần so với năm 2023 (66 báo cáo).
- Bệnh viện Từ Dũ được Trung tâm DI&ADR quốc gia xếp hạng 8/991 cơ sở khám chữa bệnh có hoạt động theo dõi ADR hiệu quả trong báo cáo tổng kết ADR quốc gia vào tháng 9/2024.
1.1. Phân bố báo cáo ADR theo tháng
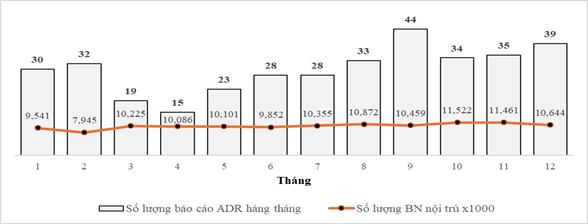
Hình 2. Phân bố báo cáo ADR theo tháng và số lượng bệnh nhân nội trú năm 2024
Số lượng báo cáo ADR nội trú phân bố theo tháng không tương ứng với số lượng bệnh nhân nội trú ở một số tháng (Hình 2). Tháng 2 và tháng 3 có số lượng bệnh nội trú tương đối cao, tuy nhiên lại có số lượng báo cáo ADR thấp nhất.
1.2. Phân bố báo cáo ADR theo khoa
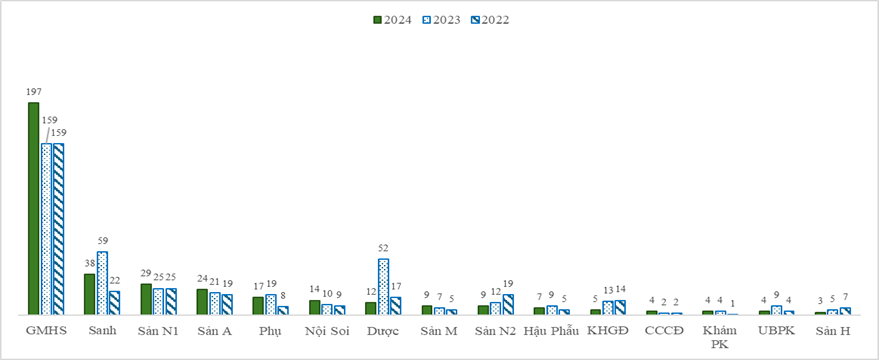
Hình 3. Số báo cáo ADR theo từng khoa phòng trong 3 năm
Có sự biến động liên tục theo từng năm về số lượng báo cáo ADR ở các khoa lâm sàng:
- Khoa Gây mê hồi sức luôn có số lượng báo cáo cao nhất trong 03 năm 2022-2024 tại bệnh viện. Trong năm 2024, khoa có 197 báo cáo (chiếm tỉ lệ 52,4%) và tăng 1,2 lần so với năm 2023 và năm 2022.
- Khoa Dược và khoa Sanh có sự giảm về số lượng báo cáo ADR năm 2024 so với năm 2023. Cụ thể, số lượng báo cáo ADR tại khoa Dược giảm 4,3 lần; khoa Sanh giảm 1,6 lần so với năm 2023.
- Trong 2 năm gần đây, số lượng báo cáo ADR ghi nhận được từ các khoa Sản A-B, Sản N1 và Nội soi có sự gia tăng nhẹ.
1.3. Phân bố báo cáo ADR theo người báo cáo
Đối tượng báo cáo ADR năm 2024 chủ yếu là Bác sĩ với tỉ lệ là 59,6% (224 báo cáo), đa phần được thực hiện bởi các Bác sĩ khoa Gây mê hồi sức với tỉ lệ là 87,9% (197 báo cáo).
Bảng 1. Số báo cáo ADR theo đối tượng báo cáo trong 3 năm
|
Đối tượng |
Tỷ lệ (%) năm 2024 |
Tỉ lệ (%) năm 2023 |
Tỉ lệ (%) năm 2022 |
|
Bác sĩ |
59,6 |
50,2 |
53,5 |
|
Hộ sinh |
36,7 |
36,1 |
40,8 |
|
Dược sĩ |
3,2 |
12,7 |
5,1 |
|
Kĩ thuật viên |
0,0 |
0,2 |
0,6 |
|
Cử nhân/ Điều dưỡng |
0,5 |
0,2 |
0,0 |
2. Phân loại báo cáo ADR trong năm 2024
2.1. Theo nhóm dược lý
Phân bố số báo cáo ADR theo nhóm dược lý trong năm 2024 được trình bày ở Bảng 2.
Bảng 2. Phân bố số báo cáo ADR theo nhóm dược lý
|
STT |
Nhóm thuốc |
Số báo cáo ADR |
Tỷ lệ (%) |
|
1 |
Kháng sinh |
193 |
51,1 |
|
2 |
Giảm đau, hạ sốt |
123 |
32,5 |
|
3 |
Thuốc thúc đẻ, cầm máu sau đẻ |
19 |
5,0 |
|
4 |
Thuốc giãn cơ, giải giãn cơ |
5 |
1,3 |
|
5 |
Thuốc điều trị ung thư |
4 |
1,1 |
|
6 |
Thuốc gây tê, gây mê |
3 |
0,8 |
|
7 |
Thuốc kháng sinh, kháng nấm đặt âm đạo |
3 |
0,8 |
|
8 |
Thuốc điều trị thiếu máu |
3 |
0,8 |
|
9 |
Thực phẩm chức năng |
2 |
0,5 |
|
10 |
Sản phẩm hỗ trợ điều trị viêm nhiễm phụ khoa |
1 |
0,2 |
|
11 |
Thuốc tẩy trùng và sát khuẩn |
1 |
0,2 |
|
12 |
Khác |
21 |
5,7 |
|
|
Tổng |
378 |
100 |
Kháng sinh là nhóm thuốc có tỷ lệ báo cáo ADR nhiều nhất, chiếm tỷ lệ 51,1% (193 báo cáo). Trong đó, thuốc Cefazolin 1g (Cefazolin natri) và Cefovidi 1g (Cefotaxime natri) có tỉ lệ báo cáo cao nhất, lần lượt là 23,3% (45 báo cáo) và 12,4% (24 báo cáo).
Tiếp theo là nhóm thuốc giảm đau hạ sốt chiếm tỷ lệ 32,5% (123 báo cáo). Trong đó, đa số là các báo cáo ADR liên quan đến thuốc Elaria 100mg (Diclofenac natri) và Diclofenac 100mg (Diclofenac natri), với tỉ lệ lần lượt là 38,2% (47 báo cáo) và 37,4% (46 báo cáo).
Các thuốc có tỉ lệ báo cáo ADR nhiều nhất, cũng là các thuốc có số lượng sử dụng nhiều nhiều nhất tại bệnh viện.
2.2. Theo nhóm thuốc có nguy cơ cao gây ADR
Có 32 báo cáo ADR xảy ra liên quan đến thuốc thuộc nhóm thuốc nguy cơ cao gây ADR. Trong đó, có 01 trường hợp xảy ra với thuốc Vinphatoxin 5IU/ml ở mức độ đe doạ tính mạng.
Bảng 3. Các báo cáo ADR của thuốc liên quan đến thuốc thuộc nhóm nguy cơ cao gây ADR
|
STT |
Thuốc gây ADR |
Số trường hợp |
Mức độ ảnh hưởng |
|
Thuốc gây tê, gây mê |
|||
|
1 |
Fresofol 1% 10mg/ml (Propofol) |
1 |
Không nghiêm trọng |
|
2 |
Lidocain 40mg/2ml (Lidocain hydroclorid) |
1 |
Không nghiêm trọng |
|
3 |
Morphin 10mg/ml (Morphin hydrochlorid) |
1 |
Không nghiêm trọng |
|
Thuốc giãn cơ, giải giãn cơ |
|||
|
4 |
Atracurium-Hameln 10mg/ml (Atracurium besilate) |
1 |
Đe doạ tính mạng |
|
5 |
Rocuronium Kabi 10mg/ml (Rocuronium bromide) |
1 |
Không nghiêm trọng |
|
6 |
Vincurium 25mg/2,5ml (Atracurium besylat) |
3 |
Không nghiêm trọng |
|
Thuốc điều trị ung thư và điều hòa miễn dịch |
|||
|
7 |
Bocartin 150mg/15ml (Carboplatin) |
2 |
Không nghiêm trọng |
|
8 |
Canpaxel 100 mg (Paclitaxel) |
2 |
Không nghiêm trọng |
|
Thuốc thúc đẻ, cầm máu sau đẻ |
|||
|
9 |
Endoprost 125mcg (Carboprost tromethamin) |
1 |
Không nghiêm trọng |
|
10 |
Heraprostol 200mcg (Misoprostol) |
9 |
Không nghiêm trọng |
|
11 |
Oxytocin 5IU/ml (Oxytocin) |
1 |
Không nghiêm trọng |
|
12 |
Vinphatoxin 10IU/ml (Oxytocin) |
2 |
Không nghiêm trọng |
|
13 |
Vinphatoxin 5IU/ml (Oxytocin) |
6 |
- 01 báo cáo đe doạ tính mạng - 05 báo cáo không nghiêm trọng |
|
Thuốc tác động lên quá trình đông máu |
|||
|
14 |
Gemapaxane 6000IU/0,6ml (Enoxaparin natri) |
1 |
Không nghiêm trọng |
2.3. Theo mức độ nghiêm trọng của phản ứng
Trong năm 2024, có 14 báo cáo ADR của Bệnh viện Từ Dũ ghi nhận ở mức độ đe doạ tính mạng (Bảng 4). Trong đó, ghi nhận 1/14 bệnh nhân có tiền sử dị ứng kháng sinh Cephalexin và trái cây ngọt; 13/14 trường hợp còn lại không ghi nhận tiền sử dị ứng thuốc, thức ăn.
Bảng 4. Các báo cáo ADR có mức độ đe doạ tính mạng
|
Nhóm thuốc |
Số báo cáo ADR có mức độ đe doạ tính mạng |
Phân tích |
|
Kháng sinh |
10 |
90% các báo cáo ADR liên quan đến kháng sinh đều là kháng sinh nhóm β-lactam, 10% còn lại không rõ nguyên nhân gây ADR: - Cefovidi 1g (Cefotaxime natri): 3 báo cáo - Cefazolin 1g (Cefazolin): 2 báo cáo - Zoliicef 1g (Cefazolin natri)): 2 báo cáo - Cefazolin 2g (Cefazolin): 1 báo cáo - Tazopelin 4,5g (Piperacillin- Tazobactam): 1 báo cáo - 1 báo cáo liên quan đến: Azilyo 500mg (Azithromycin) và Zoliicef 1g (Cefazolin natri) |
|
Thuốc thúc đẻ, cầm máu sau đẻ |
1 |
1 báo cáo liên quan đến Vinphatoxin 5IU/ml (Oxytocin) |
|
Thuốc giãn cơ, thuốc giải giãn cơ |
1 |
1 báo cáo liên quan đến Atracurium Hameln 10mg/ml (Atracurium) |
|
Thuốc giảm đau, hạ sốt, chống viêm không steroid |
1 |
1 báo cáo liên quan đến Diclofenac 100mg (Diclofenac natri) |
|
Dị nguyên không rõ loại |
1 |
01 báo cáo liên quan đến các thuốc sau: - Bridion Inj 100mg/ml (Sugammadex natri) - Acupan (Nefopam hydrochloride) |
2.4. Theo tiền căn dị ứng thuốc
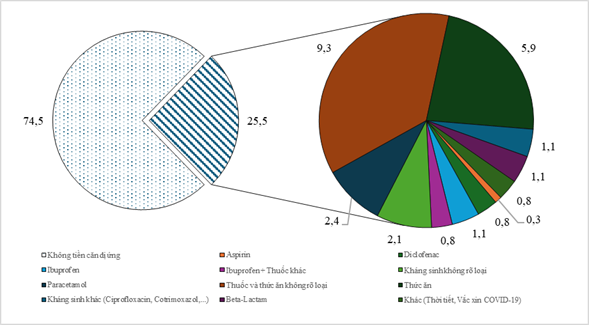
Hình 4. Phân bố báo cáo ADR theo tiền căn dị ứng thuốc
25,5% (96 báo cáo) có ghi nhận tiền căn dị ứng thuốc trên bệnh nhân, tỉ lệ này tăng 3,0% so với năm 2023 (92 báo cáo). Phân tích các trường hợp xảy ra ADR trên những bệnh nhân có tiền căn dị ứng thuốc, 36,5% (35 báo cáo) ADR xảy ra trên những người bệnh đã cung cấp thông tin về tiền căn dị ứng thuốc không rõ loại, tỉ lệ này giảm so với năm 2023 là 44,6% (41 báo cáo).
Một số trường hợp xảy ra ADR do chỉ định thuốc có chứa thành phần mà người bệnh đã cung cấp thông tin bản thân có tiền căn dị ứng:
Bảng 5. ADR do chỉ định thuốc có chứa thành phần mà người bệnh đã cung cấp thông tin
bản thân có tiền căn dị ứng
|
Thuốc gây ADR |
Tiền căn dị ứng |
Số trường hợp |
Triệu chứng |
Mức độ ảnh hưởng |
|
Thuốc kháng sinh, kháng nấm đặt âm đạo |
||||
|
Canvey (Metronidazol 225mg + Chloramphenicol 100mg + Nystatin 75mg + Dexamethason acetat 0,5mg) |
Dị ứng với triệu chứng tương tự với Safaria (Metronidazol, Chloramphenicol, Nystatin) 3 tháng trước |
1 |
Ngứa kèm đỏ da 02 tay, 02 chân. Chân phù nhẹ. |
Không nghiêm trọng |
|
Thuốc giảm đau, hạ sốt, kháng viêm không steroid |
||||
|
Paracetamol Kabi AD 10mg/ml (Paracetamol) |
Dị ứng paracetamol |
1 |
Ngứa da, nổi mề đay toàn thân. |
Không nghiêm trọng |
|
Protamol (Ibuprofen 200mg + Paracetamol 325mg) |
Dị ứng paracetamol 500mg |
1 |
Phù 02 mí mắt. |
Không nghiêm trọng |
3. Kết quả giám sát việc thực hiện quy trình giám sát phản ứng có hại của thuốc tại các khoa/phòng
Kết quả giám sát hoạt động theo dõi phản ứng có hại của thuốc từ tháng 01/2024 đến tháng 12/2024 theo “Quy trình giám sát phản ứng có hại của thuốc” (BVTD-QT-D-06), phiên bản 5.0 được phê duyệt ngày 21/12/2023: 93,4% (353/378 báo cáo) đạt tuân thủ thực hiện ở Bước 3 “Lập báo cáo ADR” (Bảng 6).
Bảng 6. Nội dung “Không đạt” theo quy trình “Giám sát phản ứng có hại của thuốc”
|
STT |
Nội dung thực hiện “Không đạt” |
Số lượng |
|
Bước 3 “Lập báo cáo ADR” |
||
|
1 |
Người báo cáo không ghi nhận thông tin về thuốc nghi ngờ gây ADR bao gồm: Tên thuốc gốc và tên thương mại, dạng bào chế, hàm lượng, nhà sản xuất, số lô, hạn dùng, liều dùng một lần, số lần dùng, đường dùng, ngày điều trị, lý do dùng thuốc. |
15 báo cáo |
|
2 |
Thiếu thông tin số lô thuốc |
06 báo cáo |
|
3 |
Sai thông tin số lô thuốc |
01 báo cáo |
|
4 |
Thiếu hàm lượng thuốc |
01 báo cáo |
|
5 |
Thiếu liều dùng |
01 báo cáo |
|
6 |
Không có thông tin người báo cáo ADR |
01 báo cáo |
Nhân viên chuyên trách của khoa Dược đã kịp thời bổ sung đầy đủ các thông tin cần thiết và phản hồi cho khoa lâm sàng trước khi tổng hợp các báo cáo gửi về Trung tâm DI & ADR quốc gia.
4. Kết quả giám sát thuốc kháng dị ứng tại các khoa lâm sàng
Kết quả giám sát thuốc kháng dị ứng và số lượng báo cáo ADR tại các khoa lâm sàng trong năm 2024 được trình bày trong Bảng 7.
Bảng 7. Kết quả giám sát thuốc kháng dị ứng tại các khoa lâm sàng
|
STT |
Khoa |
Số bệnh nhân sử dụng thuốc kháng dị ứng |
Số BN truyền máu |
Số báo cáo ADR |
||||
|
Chlorpheniramin |
Hydro-cortison |
Methyl-prednisolon |
Adrenalin |
Diphenhydramin |
||||
|
1 |
GMHS |
4 |
34 |
228 |
28 |
179 |
95 |
197 |
|
2 |
Khoa Sanh |
39 |
7 |
20 |
42 |
17 |
9 |
38 |
|
3 |
Sản A-B |
339 |
23 |
88 |
2 |
3 |
41 |
24 |
|
4 |
Khoa Phụ |
103 |
29 |
16 |
2 |
5 |
47 |
17 |
|
5 |
Sản N1 |
153 |
30 |
14 |
5 |
3 |
9 |
29 |
|
6 |
Hậu phẫu |
76 |
11 |
76 |
0 |
1 |
20 |
7 |
|
7 |
Sản N2 |
143 |
8 |
6 |
0 |
2 |
9 |
9 |
|
8 |
Sản M |
51 |
15 |
19 |
0 |
2 |
6 |
9 |
|
9 |
Nội soi |
158 |
22 |
17 |
1 |
2 |
13 |
14 |
|
10 |
KPK |
0 |
0 |
0 |
0 |
0 |
0 |
4 |
|
11 |
CCCĐ |
0 |
0 |
0 |
0 |
0 |
0 |
4 |
|
12 |
UBPK |
43 |
195 |
1498 |
2 |
1115 |
269 |
4 |
|
13 |
Sản H |
28 |
5 |
9 |
1 |
1 |
3 |
3 |
|
14 |
KHGĐ |
0 |
0 |
0 |
0 |
0 |
0 |
5 |
|
15 |
CSTS |
0 |
0 |
0 |
0 |
0 |
0 |
0 |
|
16 |
CĐHA |
0 |
0 |
0 |
0 |
0 |
0 |
0 |
Xét một số thuốc xử trí phổ biến tại bệnh viện trong trường hợp xảy ra ADR, phần lớn có sự tương xứng giữa số lượng sử dụng adrenalin với số lượng báo cáo ADR.
Đối với hydrocortison, kết quả phân tích sự tương xứng giữa số lượng báo cáo ADR với số lượng sử dụng tại các khoa lâm sàng được trình bày trong Bảng 8.
Bảng 8. Phân tích sử dụng hydrocortison tại các khoa lâm sàng năm 2024
|
STT |
Khoa sử dụng |
Phân tích sử dụng hydrocortison |
||||
|
Số lượng sử dụng |
Số BN truyền máu |
Báo cáo ADR |
Lý do khác* |
Có thể xảy ra ADR nhưng chưa thực hiện báo cáo** |
||
|
1 |
Hậu phẫu |
11 |
1 |
2 |
8 |
1 |
|
2 |
Gây mê hồi sức |
34 |
13 |
1 |
19 |
1 |
|
3 |
Nội soi |
22 |
4 |
6 |
8 |
4 |
|
4 |
Phụ |
29 |
12 |
4 |
4 |
9 |
|
5 |
Sản A-B |
23 |
6 |
2 |
13 |
2 |
|
6 |
Sản H |
5 |
1 |
1 |
2 |
1 |
|
7 |
Sản M |
15 |
2 |
2 |
10 |
1 |
|
8 |
Sản N1 |
30 |
4 |
14 |
6 |
6 |
|
9 |
Sản N2 |
8 |
3 |
2 |
0 |
3 |
|
10 |
Sanh |
7 |
2 |
1 |
3 |
1 |
* : Cường giáp, nhiễm độc giáp, lupus ban đỏ có/không biến chứng thận, bệnh lý đường hô hấp (hen suyển, hen phế quản), sốc nhiễm trùng,…
**: Xét các trường hợp đổi thuốc, ngưng thuốc sau khi dùng kháng dị ứng; trường hợp sử dụng ≥ 02 thuốc dùng để xử trí ADR
Qua phân tích, cho thấy:
- Khoa Phụ có 29 BN sử dụng hydrocortison, có 09 trường hợp có thể đã xảy ra ADR sử dụng hydrocortison để xử trí, nhưng chưa được báo cáo về đơn vị Thông tin thuốc – ADR.
- Tương tự, khoa Sản N1 có 30 BN sử dụng hydrocotison, có 06 trường hợp có thể đã xảy ra ADR sử dụng hydrocortison để xử trí, nhưng chưa được báo cáo. Khoa Nội soi có 22 BN sử dụng hydrocortison, trong đó có 04 trường hợp có thể sử dụng hydrocortison để xử trí ADR, nhưng chưa được báo cáo về đơn vị Thông tin thuốc – ADR.
5. Tóm tắt
- Số lượng báo cáo ADR được gửi về Đơn vị ADR tại Bệnh viện Từ Dũ trong năm 2024 là 378 báo cáo, giảm 7,9% so với năm 2023 và tăng 14,2% so với năm 2022.
- Trong đó, khoa Gây mê hồi sức, khoa Sanh và Sản N1 là 03 khoa có số ca báo cáo ADR cao nhất, với tỷ lệ lần lượt là: 52,1%, 10,1% và 7,7%.
- Kháng sinh là nhóm thuốc có tỉ lệ báo cáo ADR nhiều nhất: 51,1% (193 báo cáo). 90,0% trường hợp ADR ở mức độ nghiêm trọng liên quan đến kháng sinh là kháng sinh thuộc nhóm β-lactam.
Báo cáo hoạt động theo dõi adr năm 2025 của Bệnh viện Từ Dũ
Phức hợp kháng thể – thuốc (antibody–drug conjugates, ADC) hiện là một trong những bước tiến quan trọng trong điều trị ung thư vú giai đoạn sớm hoặc di căn với những biến đổi HER2 (yếu tố tăng trưởng biểu bì ở người), được chứng minh về đáp ứng, thời gian sống còn và độ an toàn. Với hiệu quả ngày càng tăng của ADC trong ung thư vú với HER2 dương tính (HER2+), nhiều tranh luận đang diễn ra xoay quanh việc kết hợp và trình tự điều trị tối ưu, cũng như những nghiên cứu mở rộng cho các thuốc khác.
Bệnh trào ngược dạ dày thực quản (GERD) với các triệu chứng ợ nóng, buồn nôn … rất phổ biến trong thai kỳ, ảnh hưởng 30- 80% phụ nữ mang thai (1). Với tần suất và mức độ nghiêm trọng của các triệu chứng tăng lên vào cuối thai kỳ. Mục tiêu điều trị là làm giảm các triệu chứng cho thai phụ mà không gây hại cho thai nhi.
Có ba loại muối tiêm benzylpenicillin cần được phân biệt rõ. Ba loại muối này không thể thay thế cho nhau về mặt lâm sàng.
- Benzylpenicillin natri
- Benzathin benzylpenicillin
- Procain benzylpenicillin
Vitamin D đóng vai trò quan trọng trong sức khỏe thai kỳ và sự phát triển của trẻ. Thiếu vitamin D trong giai đoạn mang thai liên quan đến nhiều nguy cơ bất lợi đối với mẹ và thai nhi. Các hướng dẫn mới hiện nay khuyến cáo phụ nữ mang thai nên được bổ sung vitamin D, mặc dù mức nồng độ tối ưu vẫn chưa được thống nhất.
Tiền đái tháo đường đang gia tăng nhanh và có thể tiến triển thành đái tháo đường tuýp 2 cũng như các biến chứng tim mạch nếu không được can thiệp kịp thời. Dinh dưỡng là yếu tố then chốt trong điều hòa đường huyết, trong đó việc đánh giá tác động của thực phẩm nguyên vẹn lên các chỉ số chuyển hoá ngày càng được quan tâm.



